Во сферата на модерната медицина, антибиотиците се покажаа како еден од најзначајните достигнувања, драматично намалувајќи ја инциденцата и стапката на морталитет поврзани со микробни инфекции. Нивната способност да ги променат клиничките исходи од бактериските инфекции го продолжи животниот век на безброј пациенти. Антибиотиците се критични во сложените медицински процедури, вклучувајќи операции, поставување импланти, трансплантации и хемотерапија. Сепак, појавата на патогени отпорни на антибиотици е сè поголема загриженост, намалувајќи ја ефикасноста на овие лекови со текот на времето. Случаи на отпорност на антибиотици се документирани во сите категории антибиотици како што се случуваат микробни мутации. Притисокот на селекција што го вршат антимикробните лекови придонесе за порастот на отпорните соеви, претставувајќи значаен предизвик за глобалното здравје.
За борба против итното прашање на антимикробна резистенција, од суштинско значење е да се спроведат ефикасни политики за контрола на инфекциите што го ограничуваат ширењето на резистентни патогени, заедно со намалувањето на употребата на антибиотици. Понатаму, постои итна потреба од алтернативни методи на лекување. Хипербаричната кислородна терапија (HBOT) се појави како ветувачки метод во овој контекст, вклучувајќи инхалација на 100% кислород на специфични нивоа на притисок во одреден временски период. Позиционирана како примарен или дополнителен третман за инфекции, HBOT може да понуди нова надеж во лекувањето на акутни инфекции предизвикани од патогени резистентни на антибиотици.
Оваа терапија сè повеќе се применува како примарен или алтернативен третман за различни состојби, вклучувајќи воспаление, труење со јаглерод моноксид, хронични рани, исхемични заболувања и инфекции. Клиничките примени на HBOT во третманот на инфекции се длабоки, обезбедувајќи непроценливи предности за пациентите.

Клинички апликации на хипербарична кислородна терапија кај инфекции
Сегашните докази цврсто ја поддржуваат примената на HBOT, и како самостоен и како дополнителен третман, што претставува значајни придобивки за инфицираните пациенти. За време на HBOT, притисокот на кислород во артериската крв може да се зголеми до 2000 mmHg, а резултирачкиот висок градиент на притисок кислород-ткиво може да ги зголеми нивоата на кислород во ткивата до 500 mmHg. Ваквите ефекти се особено вредни за промовирање на заздравувањето на воспалителните реакции и микроциркулаторните нарушувања забележани во исхемични средини, како и во управувањето со компартмент синдромот.
HBOT може да влијае и на состојбите што зависат од имунолошкиот систем. Истражувањата покажуваат дека HBOT може да ги потисне автоимуните синдроми и имунолошките одговори предизвикани од антигени, помагајќи во одржувањето на толеранцијата на графтот со намалување на циркулацијата на лимфоцити и леукоцити, а воедно и модулирање на имунолошките одговори. Дополнително, HBOTподдржува лекувањекај хронични кожни лезии преку стимулирање на ангиогенезата, критичен процес за подобрено закрепнување. Оваа терапија, исто така, го поттикнува формирањето на колагенска матрица, суштинска фаза во заздравувањето на раните.
Посебно внимание мора да се посвети на одредени инфекции, особено на длабоки и тешки за лекување инфекции како што се некротизирачки фасциитис, остеомиелитис, хронични инфекции на меките ткива и инфективен ендокардитис. Една од најчестите клинички примени на HBOT е за инфекции на кожата и меките ткива и остеомиелитис поврзани со ниски нивоа на кислород, кои често се предизвикани од анаеробни или резистентни бактерии.
1. Инфекции на дијабетично стапало
Дијабетично стапалоЧировите се распространета компликација кај дијабетичните пациенти, кои зафаќаат до 25% од оваа популација. Инфекциите често се јавуваат кај овие чирови (сочинуваат 40%-80% од случаите) и доведуваат до зголемен морбидитет и морталитет. Инфекциите на дијабетичното стапало (ДДИ) обично се состојат од полимикробни инфекции со идентификувани различни анаеробни бактериски патогени. Различни фактори, вклучувајќи дефекти во функцијата на фибробластите, проблеми со формирањето на колаген, механизми на клеточен имунитет и функција на фагоцитите, можат да го попречат заздравувањето на раните кај дијабетичните пациенти. Неколку студии ја идентификуваа нарушената оксигенација на кожата како силен фактор на ризик за ампутации поврзани со ДДИ.
Како една од моменталните опции за третман на DFI, Пријавено е дека HBOT значително ги зголемува стапките на заздравување на чиреви на дијабетично стапало, со што се намалува потребата од ампутации и комплицирани хируршки интервенции. Не само што ја минимизира потребата од процедури што бараат многу ресурси, како што се операции со клапни и трансплантација на кожа, туку претставува и пониски трошоци и минимални несакани ефекти во споредба со хируршките опции. Студија од Чен и сор. покажа дека повеќе од 10 сесии на HBOT довеле до подобрување од 78,3% во стапките на заздравување на раните кај пациенти со дијабетес.
2. Некротизирачки инфекции на меките ткива
Некротизирачките инфекции на меките ткива (НСТИ) често се полимикробни, обично произлегуваат од комбинација на аеробни и анаеробни бактериски патогени и често се поврзани со производство на гасови. Иако НСТИ се релативно ретки, тие имаат висока стапка на смртност поради нивната брза прогресија. Навремената и соодветна дијагноза и третман се клучни за постигнување поволни исходи, а HBOT е препорачан како дополнителен метод за справување со НСТИ. Иако сè уште постои спор околу употребата на HBOT кај НСТИ поради недостаток на проспективни контролирани студии,доказите сугерираат дека може да биде во корелација со подобрени стапки на преживување и зачувување на органите кај пациенти со NSTIРетроспективна студија покажа значително намалување на стапките на смртност кај пациенти со NSTI кои примаат HBOT.
1.3 Инфекции на хируршкото место
SSIs можат да се класифицираат врз основа на анатомското место на инфекцијата и можат да произлезат од различни патогени, вклучувајќи и аеробни и анаеробни бактерии. И покрај напредокот во мерките за контрола на инфекции, како што се техниките на стерилизација, употребата на профилактички антибиотици и подобрувањата во хируршките практики, SSIs остануваат постојана компликација.
Еден значаен преглед ја испитува ефикасноста на хипербарскиот болен хипербарски третман (HBOT) во спречувањето на длабоки инфекции на дебелото црево (SSI) при невромускулна хирургија на сколиоза. Преоперативниот хипербарски болен третман (HBOT) може значително да ја намали инциденцата на SSI и да го олесни заздравувањето на раните. Оваа неинвазивна терапија создава средина каде што нивоата на кислород во ткивата на раната се покачени, што е поврзано со оксидативното дејство на уништување на патогените. Дополнително, таа се справува со намалените нивоа на кислород во крвта и кислород што придонесуваат за развој на SSI. Покрај другите стратегии за контрола на инфекции, хипербарскиот болен хипербарски третман е препорачан особено за чисти контаминирани операции, како што се колоректалните процедури.
1.4 Изгореници
Изгорениците се повреди предизвикани од екстремна топлина, електрична струја, хемикалии или зрачење и можат да предизвикаат висока морбидитет и смртност. HBOT е корисен во лекувањето на изгореници со зголемување на нивоата на кислород во оштетените ткива. Додека студиите на животни и клиничките студии покажуваат мешани резултати во врска соЕфективноста на HBOT во третманот на изгореници, студија во која учествувале 125 пациенти со изгореници покажала дека хипербарскиот третман со изгореници (HBOT) не покажал значително влијание врз стапките на смртност или бројот на извршени операции, но го намалил просечното време на заздравување (19,7 дена во споредба со 43,8 дена). Интегрирањето на HBOT со сеопфатно управување со изгореници би можело ефикасно да ја контролира сепсата кај пациенти со изгореници, што доведува до пократко време на заздравување и намалена потреба од течности. Сепак, потребни се понатамошни обемни проспективни истражувања за да се потврди улогата на HBOT во управувањето со обемни изгореници.
1.5 Остеомиелитис
Остеомиелитис е инфекција на коската или коскената срцевина, често предизвикана од бактериски патогени. Лекувањето на остеомиелитисот може да биде предизвикувачко поради релативно слабото снабдување со крв на коските и ограниченото пенетрација на антибиотиците во коскената срцевина. Хроничниот остеомиелитис се карактеризира со перзистентни патогени, благо воспаление и некротично формирање на коскено ткиво. Рефракторниот остеомиелитис се однесува на хронични инфекции на коските кои продолжуваат или се повторуваат и покрај соодветниот третман.
Докажано е дека HBOT значително ги подобрува нивоата на кислород во инфицираните коскени ткива. Бројни серии на случаи и кохортни студии покажуваат дека HBOT ги подобрува клиничките исходи кај пациенти со остеомиелитис. Се чини дека делува преку различни механизми, вклучувајќи зголемување на метаболичката активност, сузбивање на бактериските патогени, подобрување на ефектите на антибиотиците, минимизирање на воспалението и поттикнување на заздравувањето.процеси. По HBOT, 60% до 85% од пациентите со хроничен, рефракторен остеомиелитис покажуваат знаци на супресија на инфекцијата.
1.6 Габични инфекции
Глобално, над три милиони лица страдаат од хронични или инвазивни габични инфекции, што доведува до над 600.000 смртни случаи годишно. Исходите од третманот на габични инфекции често се компромитирани поради фактори како што се променетиот имунолошки статус, основните болести и карактеристиките на вирулентноста на патогенот. HBOT станува привлечна терапевтска опција кај тешки габични инфекции поради неговата безбедност и неинвазивна природа. Студиите покажуваат дека HBOT може да биде ефикасен против габични патогени како што се Aspergillus и Mycobacterium tuberculosis.
HBOT промовира антифунгални ефекти со инхибирање на формирањето на биофилм на Aspergillus, со зголемена ефикасност забележана кај соеви на кои им недостасуваат гени за супероксид дисмутаза (SOD). Хипоксичните услови за време на габични инфекции претставуваат предизвици за испорака на антифунгални лекови, што ги прави зголемените нивоа на кислород од HBOT потенцијално корисна интервенција, иако се потребни понатамошни истражувања.
Антимикробни својства на HBOT
Хипероксичната средина создадена од HBOT иницира физиолошки и биохемиски промени кои ги стимулираат антибактериските својства, што го прави ефикасна дополнителна терапија за инфекција. HBOT покажува извонредни ефекти против аеробни бактерии и претежно анаеробни бактерии преку механизми како што се директна бактерицидна активност, подобрување на имунолошките одговори и синергистички ефекти со специфични антимикробни агенси.
2.1 Директни антибактериски ефекти на HBOT
Директниот антибактериски ефект на HBOT во голема мера се припишува на генерирањето на реактивни кислородни видови (ROS), кои вклучуваат супероксидни анјони, водород пероксид, хидроксилни радикали и хидроксилни јони - сите од кои се јавуваат за време на клеточниот метаболизам.
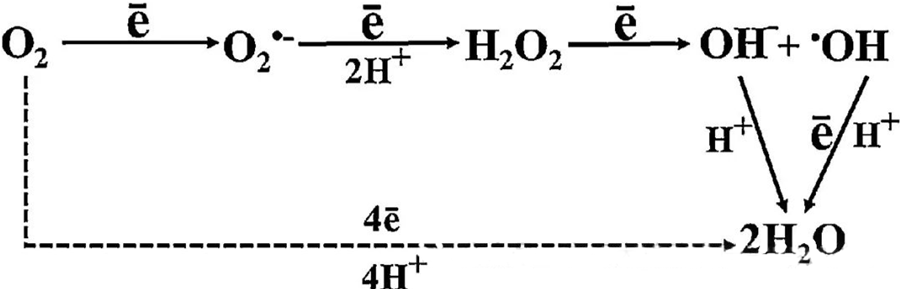
Интеракцијата помеѓу O₂ и клеточните компоненти е од суштинско значење за разбирање на тоа како се формираат ROS во клетките. Под одредени услови наречени оксидативен стрес, рамнотежата помеѓу формирањето на ROS и неговата деградација е нарушена, што доведува до зголемени нивоа на ROS во клетките. Производството на супероксид (O₂⁻) е катализирано од супероксид дисмутаза, која последователно го претвора O₂⁻ во водород пероксид (H₂O₂). Оваа конверзија е дополнително засилена со Фентонова реакција, која го оксидира Fe²⁺ за да генерира хидроксилни радикали (·OH) и Fe³⁺, со што се иницира штетна редокс секвенца на формирање на ROS и клеточно оштетување.
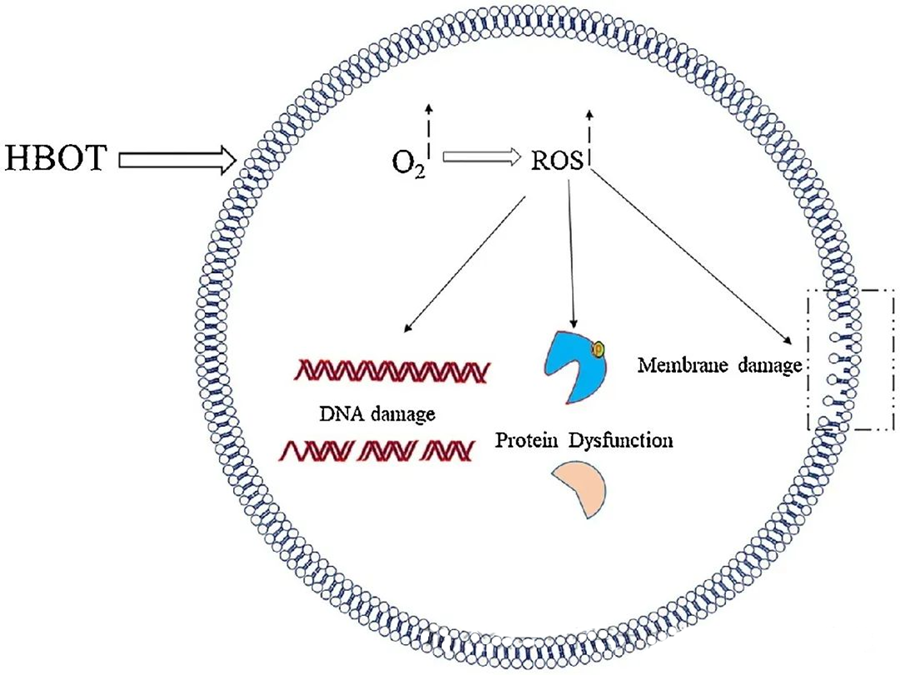
Токсичните ефекти на ROS ги таргетираат критичните клеточни компоненти како што се ДНК, РНК, протеините и липидите. Имено, ДНК е примарна цел на H₂O₂-посредуваната цитотоксичност, бидејќи ги нарушува структурите на деоксирибозата и ги оштетува базните состави. Физичкото оштетување предизвикано од ROS се протега на хеликсот на ДНК, што потенцијално е резултат на липидна пероксидација предизвикана од ROS. Ова ги нагласува негативните последици од покачените нивоа на ROS во биолошките системи.
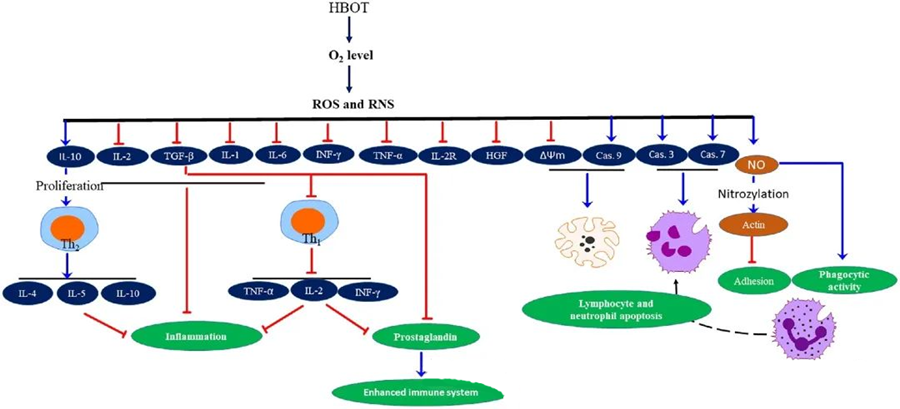
Антимикробно дејство на ROS
ROS играат витална улога во инхибирањето на растот на микробите, како што е докажано преку генерирањето на ROS предизвикано од HBOT. Токсичните ефекти на ROS директно ги таргетираат клеточните состојки како што се ДНК, протеините и липидите. Високите концентрации на активни кислородни видови можат директно да ги оштетат липидите, што доведува до пероксидација на липиди. Овој процес го нарушува интегритетот на клеточните мембрани и, следствено, функционалноста на рецепторите и протеините поврзани со мембраната.
Понатаму, протеините, кои се исто така значајни молекуларни цели на ROS, подлежат на специфични оксидативни модификации кај различни аминокиселински остатоци како што се цистеин, метионин, тирозин, фенилаланин и триптофан. На пример, покажано е дека HBOT предизвикува оксидативни промени кај неколку протеини во E. coli, вклучувајќи го факторот на елонгација G и DnaK, со што влијае на нивните клеточни функции.
Зајакнување на имунитетот преку HBOT
Антивоспалителни својства на HBOTДокументирани се, како што се покажуваат како клучни за ублажување на оштетувањето на ткивото и сузбивање на прогресијата на инфекцијата. HBOT значително влијае на експресијата на цитокини и други воспалителни регулатори, влијаејќи на имунолошкиот одговор. Различни експериментални системи забележале диференцијални промени во генската експресија и генерирањето на протеини по HBOT, кои или ги зголемуваат или намалуваат факторите на раст и цитокините.
За време на процесот на HBOT, зголемените нивоа на O₂ предизвикуваат низа клеточни реакции, како што се супресија на ослободувањето на проинфламаторни медијатори и поттикнување на апоптоза на лимфоцитите и неутрофилите. Заедно, овие дејства ги зајакнуваат антимикробните механизми на имунолошкиот систем, со што се олеснува заздравувањето од инфекции.
Понатаму, студиите сугерираат дека зголемените нивоа на O₂ за време на HBOT можат да ја намалат експресијата на проинфламаторни цитокини, вклучувајќи интерферон-гама (IFN-γ), интерлеукин-1 (IL-1) и интерлеукин-6 (IL-6). Овие промени вклучуваат и намалување на односот на CD4:CD8 Т-клетките и модулирање на други растворливи рецептори, што на крајот ги зголемува нивоата на интерлеукин-10 (IL-10), што е клучно за спротивставување на воспалението и поттикнување на заздравувањето.
Антимикробните дејства на HBOT се испреплетени со сложени биолошки механизми. И супероксидот и покачениот крвен притисок се пријавени дека неконзистентно ја промовираат антибактериската активност предизвикана од HBOT и апоптозата на неутрофилите. По HBOT, значителното зголемување на нивоата на кислород ги подобрува бактерицидните способности на неутрофилите, суштинска компонента на имунолошкиот одговор. Понатаму, HBOT ја потиснува адхезијата на неутрофилите, што е посредувано преку интеракцијата на β-интегрините на неутрофилите со меѓуклеточните адхезивни молекули (ICAM) на ендотелните клетки. HBOT ја инхибира активноста на неутрофилниот β-2 интегрин (Mac-1, CD11b/CD18) преку процес посредуван од азотен оксид (NO), придонесувајќи за миграцијата на неутрофилите кон местото на инфекцијата.
Прецизното преуредување на цитоскелетот е неопходно за неутрофилите ефикасно да ги фагоцитираат патогените. Покажано е дека S-нитрозилацијата на актинот ја стимулира полимеризацијата на актинот, потенцијално олеснувајќи ја фагоцитната активност на неутрофилите по претходниот третман со HBOT. Покрај тоа, HBOT ја промовира апоптозата во човечките Т-клеточни линии преку митохондријални патишта, при што е пријавена забрзана смрт на лимфоцитите по HBOT. Блокирањето на каспаза-9 - без влијание врз каспаза-8 - ги покажа имуномодулаторните ефекти на HBOT.
Синергистички ефекти на HBOT со антимикробни агенси
Во клиничките апликации, хипероксидниот третман со кислород (HBOT) често се користи заедно со антибиотици за ефикасна борба против инфекции. Хипероксичната состојба постигната за време на HBOT може да влијае на ефикасноста на одредени антибиотици. Истражувањата сугерираат дека специфичните бактерицидни лекови, како што се β-лактамите, флуорохинолоните и аминогликозидите, не само што дејствуваат преку вродени механизми, туку делумно се потпираат и на аеробниот метаболизам на бактериите. Затоа, присуството на кислород и метаболичките карактеристики на патогените се клучни при оценувањето на терапевтските ефекти на антибиотиците.
Значајни докази покажаа дека ниските нивоа на кислород можат да ја зголемат отпорноста на Pseudomonas aeruginosa на пиперацилин/тазобактам и дека околината со низок кислород, исто така, придонесува за зголемена отпорност на Enterobacter cloacae на азитромицин. Спротивно на тоа, одредени хипоксични состојби можат да ја зголемат бактериската чувствителност на тетрациклински антибиотици. HBOT служи како одржлив дополнителен терапевтски метод со индуцирање на аеробен метаболизам и реоксигенирање на хипоксичните инфицирани ткива, со што последователно се зголемува чувствителноста на патогените на антибиотици.
Во претклиничките студии, комбинацијата на HBOT - администрирана двапати дневно во тек на 8 часа на 280 kPa - заедно со тобрамицин (20 mg/kg/ден) значително го намали бактериското оптоварување кај инфективниот ендокардитис предизвикан од Staphylococcus aureus. Ова го демонстрира потенцијалот на HBOT како помошен третман. Понатамошните истражувања покажаа дека под 37°C и притисок од 3 ATA во тек на 5 часа, HBOT значително ги подобрил ефектите на имипенем против Pseudomonas aeruginosa инфицирана со макрофаги. Дополнително, се покажа дека комбинираниот модалитет на HBOT со цефазолин е поефикасен во лекувањето на остеомиелитис предизвикан од Staphylococcus aureus кај животински модели во споредба со самиот цефазолин.
HBOT, исто така, значително го зголемува бактерицидното дејство на ципрофлоксацинот против биофилмовите на Pseudomonas aeruginosa, особено по 90 минути изложеност. Ова подобрување се припишува на формирањето на ендогени реактивни кислородни видови (ROS) и покажува зголемена чувствителност кај мутанти со пероксидаза-дефект.
Кај модели на плеврит предизвикан од метицилин-резистентен Staphylococcus aureus (MRSA), колаборативниот ефект на ванкомицин, теикопланин и линезолид со HBOT покажа значително зголемена ефикасност против MRSA. Метронидазолот, антибиотик кој е широко користен во лекувањето на тешки анаеробни и полимикробни инфекции како што се инфекции на дијабетично стапало (DFIs) и инфекции на хируршко место (SSIs), покажа поголема антимикробна ефикасност под анаеробни услови. Идните студии се потребни за да се истражат синергистичките антибактериски ефекти на HBOT во комбинација со метронидазол и во in vivo и во in vitro услови.
Антимикробната ефикасност на HBOT врз резистентни бактерии
Со еволуцијата и ширењето на резистентни соеви, традиционалните антибиотици често ја губат својата моќ со текот на времето. Понатаму, HBOT може да се покаже како суштински во лекувањето и спречувањето на инфекции предизвикани од патогени отпорни на повеќе лекови, служејќи како критична стратегија кога третманите со антибиотици не успеваат. Бројни студии ги објавија значајните бактерицидни ефекти на HBOT врз клинички релевантните резистентни бактерии. На пример, 90-минутна сесија со HBOT на 2 ATM значително го намали растот на MRSA. Дополнително, во моделите на соодноси, HBOT ги зголеми антибактериските ефекти на разни антибиотици против MRSA инфекции. Извештаите потврдија дека HBOT е ефикасен во лекувањето на остеомиелитис предизвикан од Klebsiella pneumoniae што произведува OXA-48 без потреба од дополнителни антибиотици.
Накратко, хипербаричната кислородна терапија претставува повеќеслоен пристап кон контрола на инфекциите, подобрувајќи го имунолошкиот одговор, а воедно и засилувајќи ја ефикасноста на постојните антимикробни агенси. Со сеопфатно истражување и развој, таа има потенцијал да ги ублажи ефектите од отпорноста на антибиотици, нудејќи надеж во тековната борба против бактериските инфекции.
Време на објавување: 28 февруари 2025 година

